Validierte Prüfungen zur Vermeidung von Kontaminationsrisiken
Kontaminationen durch pharmazeutische Gase stellen eine unsichtbare Gefahr dar, die die Produktsicherheit, die Gesundheit der Patient:innen und die regulatorische Zulassung erheblich gefährden kann. Um die Produktqualität zu gewährleisten, muss die Reinheit dieser Gase kontinuierlich überwacht und streng kontrolliert werden. Die Überprüfung, ob Gase wie Stickstoff, Sauerstoff oder Kohlendioxid den Anforderungen der Pharmakopöen entsprechen, ist daher ein zentraler Bestandteil der Qualitätskontrolle.
Die Durchführung solcher Prüfungen ist jedoch anspruchsvoll: Sie erfordert validierte Probenahmeverfahren, hochspezialisierte Geräte und qualifiziertes Personal, das sowohl sicherheits- als auch qualitätsrelevante Anforderungen erfüllt.
Das Eurofins BioPharma Product Testing Netzwerk bietet pharmazeutische Gasanalysen mit der Präzision, Expertise und regulatorischen Konformität, die Ihre Prozesse erfordern. Unsere speziell ausgestatteten Labore, validierten Methoden und erfahrenen Teams helfen Ihnen, Risiken zu minimieren und höchste Qualitäts- und Sicherheitsstandards einzuhalten – insbesondere dort, wo pharmazeutische Gase während der Produktion potenzielle Kontaminationsquellen darstellen.
Typische Gase in der pharmazeutischen Industrie:
- Stickstoff zur Inertisierung oder Spülung
- Druckluft zur Spülung
- Sauerstoff für Fermentationsprozesse
- Kohlendioxid für Extraktion und Reinigung
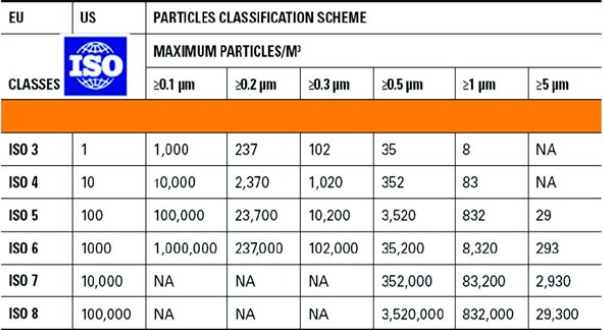
Die Qualitätsanforderungen für diese Gase sind in der Europäischen und der US-amerikanischen Pharmakopöe definiert. Zusätzlich zu den pharmakopöischen Vorgaben prüfen wir die Gase auch auf partikuläre und mikrobiologische Verunreinigungen. Die Kontamination des Gases darf dabei nicht höher sein als die des Raums, in dem es verwendet wird. Ein Gas, das z. B. in einem ISO-5-Raum (entspricht Klasse 100) eingesetzt wird, muss auch gemäß ISO-5-Spezifikationen analysiert werden. Die entsprechenden Grenzwerte für partikuläre und mikrobiologische Belastung sind in Tabelle 1 und 2 aufgeführt.
Unsere vor Ort durchgeführten Probenahmen sind vollständig validiert und gewährleisten repräsentative Gasproben. Wir stellen detaillierte Analysenzertifikate (CoA) sowie vollständige Rückverfolgbarkeit für Audits bereit.
Tabelle 1: Spezifikationen und Methoden gemäß Europäischer Pharmakopöe
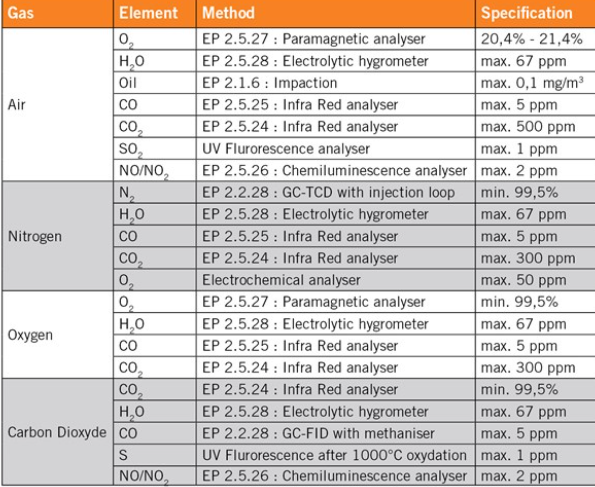
Tabelle 2: ISO-Reinraumklassifizierung – Grenzwerte für Partikelkonzentrationen